-
Products
-
실험실제품
- 미터와 프로브
- 시약과 스탠다드
-
Microbiology
Accessories and Chemicals Dehydrated Media InstrumentsLabware Prepared Media
-
온라인제품
나트륨 EZ Series Analysers
- 철
- Aluminium
- Manganese
- Phosphate
- Chloride
- Cyanide
- Fluoride
- Sulphate
- Sulphide
- Arsenic
- Chromium
- Copper
- Nickel
- Zinc
- Ammonium
- 총 질소(TN)
- 총 인(TP)
- Phenol
- Volatile Fatty Acids
- 알칼리도
- ATP
- 경도
- Toxicity
- 샘플 사전 조정
- Boron
- Colour
- Nitrate
- Nitrite
- Silica
- Hydrogen Peroxide
- EZ Series Reagents
- EZ Series Accessories
- EZ sc Series Additional Analyzers
- EZ sc Series Inorganics
- EZ sc Series Metals
- EZ sc Series Nutrients
- 온라인 제품 센서 및 컨트롤러
- Multiparameter Online Panels
-
실험실 관련 장비
General Lab Consumables Glassware/PlasticwareSafety Equipment
- 테스트 키트
- Automated Lab Systems
- Industrial UV
- Electrochemistry
-
실험실제품
- Industries
- Support
- Parameters
- WQ Platform
- About Us
Korea, South
Choose your country or region:
Europe
Americas
Asia - Australasia
- Australia
- Mainland China
- India
- Indonesia
- Japan
- Malaysia
- New Zealand
- Philippines
- Singapore
- South Korea
- Thailand (Thai)
- Taiwan
- Vietnam
Middle East - Africa
02-3484-5700
질산염 & 아질산염
질산염과 아질산염은 무엇일까요?
질산염과 아질산염은 질소 와 산소를 포함하고 있는 혼합물입니다. 질산염과 아질산염 입자 모두 하나의 질소 원자를 포함하고 있습니다. 아질산염은 두개의 산소 원자를, 질산염은 세개의 산소 원자를 가지고 있습니다.
질산염
질산염은 질소에서 더욱 산화된 상태를 나타냅니다. 독립영양체 박테리아는 암모니아를 아질산염으로 변환하고, 유산소 상태에서 질산염으로 변환합니다. 빛은 많은 양의 대기 질소(N 2)를 직접 질산염으로 변환합니다. 질산염의 박테리아 제거는 유산소 상태에서 아질산염을 만들어 냅니다.
아질산염
아질산염 질소는 암모니아/암모늄의 생물학적 분해의 중간단계에서 발생합니다. 독립영양체 박테리아는 산화(유산소) 상태에서 암모니아를 질산염으로 변환시킵니다.
질화작용 및 탈질화
이 과정은 호수, 강과 같은 물 및 자연적 환경에서 자연적으로 발생합니다. 이러한 생물학적 과정은 일반적으로 폐수 처리 또는 질소 제거를 위한 생물여과에 적용됩니다. 질화작용은 원하지 않고, 가깝게 모니터링되어야 하는 식수 분배 시스템에서 발생할 수 있습니다.
질화작용은 암모니아 가 아질산염으로, 최종적으로 질산염으로 산화되는 두 단계의 호기성 생체 산화를 말합니다. 탈질화는 질산염이 산소가 제거되어 최종단계로 입자 질소를 만들어내는 미생물적 촉진 과정입니다.
이러한 과정에서 폐수 처리의 산화(유산소) 및 무산소 구역 내 다른 조건에 따라 암모니아와 질산염 및 아질산염을 질소 가스로 변환하기 위하여 니트로소모나스와 같은 독립영양균이나 니트로박터 속과 같은 종속영양균을 사용할 수 있습니다. 산소 관리는 알칼리도와 같은 다른 중요한 요소 사이에 질화작용에 매우 중요합니다. 용존 산소(DO) 는 이 과정에서 반드시 모니터링되고 관리되어야 합니다. 효과적인 탈질화 과정은 부족한 DO와 순조로운 탄소 분해에 달려 있습니다.
아질산염과 질산염을 측정해야 하는 이유
환경에서 질소 순환의 필수적인 부분으로, 아질산염과 질산염은 식물 및 그들을 소비하는 복합 유기체에게 영양분임과 동시에 질소의 필수 원료입니다. 산소와 질소로 구성되어 있어, 질소이온은 토양에서 자연적으로 발생합니다. 아질산염은 순조롭게 질산염으로 산화되기 때문에, 표면수에서는 보통 발견되지 않습니다.
농도가 충분하게 모니터링되고 유지될 때, 질산염과 아질산염은 많은 산업 및 공공 수질 모니터링 프로그램에서 중요한 역할을 담당합니다:
- 아질산염은 산업 공정 용수 및 냉각탑에서 부식 억제제로 사용됩니다.
- 식품 산업은 방부제로 질산염을 사용합니다.
- 많은 인공 비료는 질산염 형태의 질소를 포함하고 있습니다.
과도한 질산염 및 아질산염 농도는 수처리 과정에 부정적인 영향을 끼칠 수 있고, 인간의 건강에 위협이 됩니다:
- 물 속의 질산염이 높으면 안정화의 최종 단계 또는 비료가 많이 투입된 평야로부터 지표수의 생물학적 폐기물이 있음을 의미합니다.
- 수신수로 배출되는 유출물에 질산염이 많이 포함되어 있다면, 수질을 저하시키고, 조류의 과도한 성장을 촉진합니다.
- 과도한 양의 질산염(MCL=10mg/L)을 포함하고 있는 식수는 유아들의 메트헤모글로빈 혈증(청색증)을 유발할 수 있어, 질산염의 농도는 0.1mg/L를 초과하면 안됩니다.
질산염 및 아질산염 농도는 폐수 처리 과정에 부정적인 영향을 끼치며, 건강에 위협적일 수 있습니다:
- 아질산염은 혐기성 구역의 부착물을 제거하기 위한 생물학적 인의 유지로 인하여 시스템 내 성능 저하를 일으킬 수 있습니다.
- 염소 소독 시스템의 효과는 아질산염의 존재에 의해 떨어질 수 있습니다.
- 폐수의 배출 시 포함되어 있는 총 무기 질소(TIN)는 배출되는 물의 품질 저하를 야기할 수 있습니다.
하크(Hach)에서 질산염과 아질산염을 성공적으로 모니터링하고 관리하는 데 활용할 수 있는 장비, 관련 자료, 교육 및 소프트웨어를 찾아 보시기 바랍니다.
질산염과 아질산염을 측정할 수 있는 제품 라인업
Hach의 NT3100sc UV 질산염 센서와 NT3200sc UV 질산염, 아질산염 센서는 높은 정확도, 간편한 유지관리 그리고 이중 파라미터(측정항목) 기능을 제공합니다.
자세히 보기ISENO3181 이온 선택 전극을 포함한 HQ440D 실험실용 질산염(NO3-) 이온 미터기 패키지
하크(Hach)의 HQ440D 실험실용 다항목 미터기는 측정에 대한 상식을 뛰어넘는 향상된 실험 목적의 측정기입니다.
자세히 보기
질산염/아질산염 모니터링이 요구되는 공정
폐수 처리
질소의 특정 형태가 허용되지 않는 폐수 시스템이거나 모니터링이 요구되는 시스템이라면, 시스템을 거치는 아질산염과 질산염의 농도에 대한 이해가 필요합니다.
배출되는 총질소(TN), 총 무기질소(TIN) 또는 NOx 모니터링이 요구되는 시스템은 플랜트를 통틀어 중요한 장소에서 아질산염(NO 2 -)과 질산염(NO 3 -)를 표본 조사해야 합니다.
질화작용 및 탈질화작용의 효율성 및 안정성은 많은 요소에 달려있습니다. 적절한 pH, 알칼리도, 용존산소(DO), 온도, 구할 수 있는 탄소, 고형물 체류 시간(SRT), 내부 혼합 액체 재생율(IMLR) 및 각 개별적인 생물학적 시스템을 위한 다른 요소 들 사이의 산화상태 등이 그것입니다.
질소는 암모니아(NH 3) 또는 암모늄(NH 4 +)으로 폐수에 유입되며, 생물학적 처리 과정에 의해 제거됩니다. 공공유입수의 일반적인 암모니아 질소 수준은 30mg/L 에서 50mg/L NH3-N 사이의 범위입니다. 질산염 수준은 질화 과정에서 유산소 생물학적 처리 단계에 의해 암모니아와 유기 질소가 질산염으로 전환되는 단계를 나타냅니다.
질화과정은 질화 세균의 안정적인 개체수, 적절한 산소(DO), 알칼리도, pH, 온도 및 고형물 체류 시간(SRT) 등이 있는 호기 조건에서 암모니아/암모늄을 질산염으로 전환합니다.
탈질화 과정은 질산염을 질소 가스(N 2)로 변화합니다. 질소 가스(N2)는 쉽게 생분해 가능한 적절한 탄소, 적절한 유지시간, 온도 및 자유 산소(DO)를 통해 시스템에서 제거됩니다. 만약 시스템에 탈질화 과정을 돕는 내부 재이용(IR 또는 IMLR)이 있다면, 적절한 재이용률을 모니터링해야 합니다.
무산소 구역에서 질산염을 모니터링하는 것은 탈질화 과정의 효율을 이해하는 데 중요합니다. 변동이 잦은 구역의 시스템에서, 용량은 무산소 또는 호기 스윙존의 요구조건을 가능하게 하는 지표가 될 수 있습니다.
생물학적 인 제거법(BPR)을 수행하는 시스템에서, 질산염은 혐기성 영역으로 들어가는 반송 슬러지(RAS) 흐름에서 모니터링되어야 합니다. 이 영역으로 들어가는 질산염은 생물학적 인 제거의 주요 역할을 줄이거나 중단합니다.
활성화된 슬러지 혼합액(ML)에서, 생물학적 시스템에서 두번째 정화과정으로 들어가기 전 아질산염과 질산염 모니터링은 반드시 이해되어야 합니다. 부적절한 고형물 체류 시간(SRT)은 두번째 침전에서 과도한 고형물 저지를 야기할 수 있습니다. 또한 만약 아질산염/질산염 농도가 높다면 이것은 부유 슬러지, 정화 블랭킷의 탈질화 및 높은 고형물 배출로 이어질 수 있습니다.
어떤 특정된 혐기성 박테리아는 질소 제거를 손쉽게 수행할 수 있습니다. 이러한 유형의 박테리아는 질소 제거를 위한 표준 질화과정/탈질화과정 계획을 사용하지 않습니다. 이러한 유형의 질소 제거는 일반적으로 공정의 다양한 단계에서 아질산염과 질산염의 수준이 핵심적인 측류 시스템에서 수행됩니다. 완전하지 않은 탈질화 과정은 아질산염 수요로 인한 염소 소독 비용을 증가시키는 결과로 이어질 수 있습니다.
아질산염 및 질산염 배출 모니터링은 개별 오염물질 또는 총질소(TN) 또는 총무기질소(TIN) 요구사항의 일부로 제한 수치 또는 모니터링의 항목으로 요구될 수 있습니다.

지표수, 혼합수 및 지하수
질산염은 비료의 사용으로 인해 농업 분야에서 발견되는 오염물질로, 규제대상입니다. 잠재적으로 원수를 오염시킬 수 있는 질산염 수준을 모니터링하는 것은 중요합니다. 처리가 어렵고 역삼투압(RO) 여과를 요구할 수 있기 때문입니다. 유사하게 아질산염을 모니터링하는 것도 중요합니다. 원수에 존재할 수 있기 때문입니다. 또한 처리 과정에서 아질산염은 산화되어 질산염이 될 수도 있습니다.
특히 지표수의 직접적인 영향 하에 있는 지하수(GWUDI)는 질산염과 같은 혼합물을 포함하고 있을지 모릅니다. MCL(10mg/L) 아래의 수준은 인간의 건강에 해롭지 않지만, 어떤 시스템은 처리 과정에서 어려움이 따릅니다. (특히 첫번째로 염소를 사용하는 경우).

식수 처리
아질산염이 있을 수도 있고, 처리 과정에서 산화가 발생하여 질산염을 생산할 수도 있는 원수를 모니터링하는 것은 중요합니다. 염소처리된 수돗물에서 아질산염과 질산염은 잘못된 일의 시작과, 줄이기 위하여 시간 상 오래걸리는 지속적인 질화과정을 감지하기 위해 중요합니다. 염소처리된 식수 공급 시스템에서 아질산염 농도의 변화는 질산화 과정의 조짐이 될 수 있습니다. 공공 보건을 지키기 위하여 아질산염과 질산염을 모니터링하고, 규제된 수준의 농도로 유지하는 것이 중요합니다.

질산염/아질산염을 모니터링하고 관리하는 방법

황산철 방법 (아질산염)
이 방법은 대개 폐수에 사용됩니다. 산성 매체에서 황산 제1철은 아질산염(NO 2 -)에서 질소를 제거하고, 아산화질소(NO)를 형성합니다. 철을 함유한 이온은 아산화질소와 결합하여 갈색의 양상을 보입니다. 색의 밀도는 샘플수에 존재하는 아질산염에 비례합니다. 색의 변화는 베르의 법칙을 따릅니다.
탁상용:
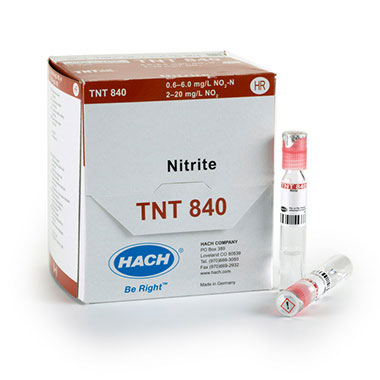
USEPA 디아조화법 (아질산염)
낮은 범위의 아질산염 시험에서 아질산 이온은 설파닐산과 반응하여 중간의 디아조늄염을 만듭니다. 이는 크로노트로픽산과 반응하여 적오렌지의 집합체를 만들어내는데 이는 아질산염의 양과 정비례합니다. 그러므로 색의 밀도 측정은 샘플 수의 아질산염 농도를 정확하게 결정할 수 있게 해줍니다. 이 방법은 폐수, 해수, 식수, 지표수 및 공정수 등에서 사용될 수 있습니다.
탁상용:
휴대용:
온라인:


크로모트로프산법 (질산염)
샘플 속의 질산염은 강한 산성 상태 하에서 크로모트르프산과 반응하여 노란색의 물체를 생성합니다. 이는 분광광도계 또는 비색계로 분석될 수 있습니다. 이러한 방법은 폐수에서 사용됩니다.
탁상용:

카드뮴 제거법 (질산염/아질산염)
이 비색법을 식수, 폐수 및 해수에서 사용하면, 질산염은 구리로 도금된 카드륨 입자와 함께 아질산염으로 환원됩니다. 그런 다음 디아조늄 시약은 아질산염과 반응하여 붉은 색을 만들어냅니다. 색의 밀도는 샘플 내에 존재하는 질산염과 아질산염의 원래 양에 비례합니다.
탁상용:
휴대용:

하이드라진 제거법 (질산염/아질산염)
식수, 폐수 및 해수에서 사용할 수 있는 이 비색법에서 질산염은 하이드라진 황산염과 아질산염으로 환원됩니다. 이후 디아조늄 시약은 아질산염과 반응하여 적색을 만들어냅니다. 색의 밀도는 샘플에 존재하는 질산염 및 아질산염의 원래 양에 비례합니다.
온라인용:
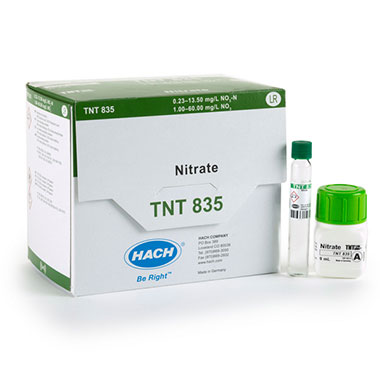
USEPA 디메틸페놀법 (질산염)
이 방법은 폐수, 식수, 지표수 및 공정수에 사용됩니다. 황산 및 인산이 포함된 용액 속 질산염 이온은 2,6-디메틸페놀과 반응하여 측정될 수 있는 4-니트로-2, 6-디메틸페놀을 형성합니다. (파장길이 345nm)
탁상용:

직접 ISE 방법 (질산염)
질산염 이온은 ISE 멤브레인에 의해 선택적으로 흡수됩니다. 흡수된 질산염 이온은 샘플 내 질산염의 농도에 비례하는 전위(전압)을 야기합니다. ISE 멤브레인은 비활성의 폴리 염화비닐(PVC) 플라스틱 매트릭스에서 질산염 이온교환체인 솔벤트-폴리머 멤브레인입니다. 이 질산염 전극은 내부에 은/염화은 성분이 있으며, 내부 채움 용액과 만나 고정된 기준의 전위를 야기합니다. 이 방법은 식수 및 폐수에 사용됩니다.
탁상용/휴대용:
온라인용:

UV 검사방법 (질산염)
첫번째 측정은 220nm에서 수행됩니다. 질산염과 유기물질은 220nm의 빛을 흡수합니다. 두번째 측정은 275nm에서 수행됩니다. 질산염은 275nm에서 흡수되지 않습니다. 유기물질에 의해 야기된 흡광도를 정정하는데 사용됩니다. 염산은 수산화 이온 또는 탄산염 이온으로부터 간섭을 막기위해 테스트 과정에 추가됩니다. 이 방법은 테스트에 방해가 될 수 있는 고농도의 유기물질을 포함하고 있는 샘플에는 권장되지 않습니다. 그러므로 이 방법은 오염되지 않은 자연수 및 음료수를 검사하는 데 사용됩니다.
탁상용:
온라인용:

질산염 & 아질산염 테스트 스트립
질산염 농도 범위는 0, 1, 2, 5, 10, 20 및 50 단계에서 0-50mg/L 이며, 아질산염은 0, 0.15, 0.3, 1, 1.5 및 3단계에서 0-3mg/L입니다.
자주 묻는 질문 (FAQ)
질산염 ISE 고체 상태 프로브는 어떻게 보관해야 합니까?
모든 고체 상태의 전극은 건조하고 뚜껑이 덮힌 채 보관되어야 합니다. 모든 고체 상태의 결합 전극은 내부에 전해액을 가지고 있습니다. 이 보관 방법 때문에, 어떤 용액(심지어 솔루션)도 전해질 사용의 촉진 및 종종 과도한 손실의 원인이 될 수 있습니다. 이것은 전해질 사용기간을 심각하게 줄일 수 있습니다. 전해질의 과도한 손실에 대한 증상은 교정 실패 및 안정화 시간이 길어지는 결과로 이어질 수 있는 커다란 시초입니다. 교정 중에 나중에 투입되는 표준용액은 이전에 투입하는 표준용액보다 안정화 시간이 더 길 수 있습니다. 이는 측정값이 안정화 되기 전에 이 포인트들을 "록인(lock-in)"할 수 있습니다. 표준용액의 조기 록인은 기울기에 문제를 야기하며, 교정 실패로 이어질 수 있습니다.
질산염/아질산염 분석을 위한 샘플은 어떻게 보존해야 할까요?
질산염 방법이 만약 보존된다면, 샘플은 현재 총 질산염+아질산염을 말합니다. 이것이 의미하는 것이 무엇일까요?
최상의 결과를 위해 샘플을 가능한 빨리 분석하십시오. 만약 즉각적인 분석이 가능하지 않다면, 샘플을 6°C 또는 42.8°F 아래에서 최대 48시간 동안 여과하고 유지하십시오. 샘플을 최대 28일 동안 지키기 위해서, 황산(~ 리터 당 2mL)과 함께 pH2 또는 그 이하로 조정하십시오. 이 때 온도는 6°C 또는 42.8°F 이하를 유지하십시오.
황산과 함께 산성화된 샘플을 보존할 때, 샘플에 있는 아질산염은 질산염으로 변환됩니다. 이러한 변환 때문에, 샘플이 분석 전에 중성화된다고 하더라도, 아질산염으로 분화하는 것이 불가능해집니다. 아질산염 분화를 요구하는 샘플은 보존될 수 없습니다.
Test N Tube(TNTplus ®) 방법 10206은 미국환경보호국(EPA)의 승인을 받은 질산염 측정법입니까?
질산염 TNTplus ® Vial Test, LR (0.2-13.5mg/L NO3-N)과 질산염 TNTplus ® Vial Test, HR (5-35 mg/L NO3 -N)에 사용되는 방법 10206 (제품번호 각 TNT835 및 TNT836)은 미국연방규정집(CFR)의 코드 40에 인용된 식수에 대한 EPA의 승인을 받았습니다. 폐수에 대해서도 40 CFR 136에서 인용된 바와 같이 EPA의 승인을 받았습니다. (미국 수질 정화법)
TNT835 및 TNT836에 대한 질산염 방법 10206은 아질산염의 간섭을 받습니까?
2.0mg/L 이상의 아질산염 농도는 TNT835 및 TNT836에서 적용되는 질산염 방법 10206을 방해합니다. (높은 바이어스 결과) 이를 처리하기 위해서는 5.0mL의 샘플에 50mg의 술팜산(아미드 술폰산)을 투입하고 용해한 다음 10분간 기다리십시오. 그리고 나서 준비된 샘플을 방법의 설명에 따라 분석하십시오.





